El Mycoplasma hyopneumoniae (M. hyopneumoniae) es el agente causal de la neumonía enzoótica porcina (NEP), una de las enfermedades respiratorias de mayor impacto en la industria porcina. M. hyopneumoniae predispone a infecciones concomitantes con otros patógenos (virus, bacterias y parásitos). El principal signo clínico de la NEP es la tos no productiva, de curso clínico crónico. Las lesiones macroscópicas consisten en áreas de consolidación pulmonar, de color violáceo-grisáceas, encontradas principalmente en los lóbulos pulmonares apicales, cardíacos, intermedio y parte anterior de los diafragmáticos, que pueden permanecer hasta la edad de faena. El impacto de la enfermedad, radica no tanto por la mortalidad sino por la disminución en la ganancia diaria de peso (GDP), ya que ha sido demostrado que por cada 10% de pulmón afectado existe una disminución en la GDP de 37,4 grs. Las lesiones microscópicas tempranas consisten en acumulación de neutrófilos en la luz alveolar y de las vías aéreas. Se observa infiltración de linfocitos alrededor de las vías aéreas. A medida que la enfermedad avanza, aumenta el número de linfocitos en el tejido perivascular, peribronquial y peribronquiolar hasta llegar a la formación de una hiperplasia linfoide bastante importante
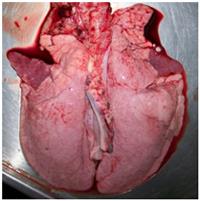
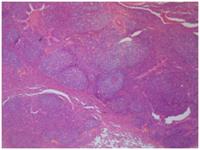
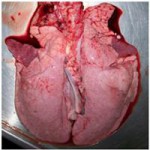
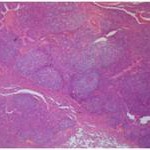
A la izquierda se observa la lesión macroscópica (4,5% de volumen pulmonar afectado, aproximadamente) de color violácea, deprimida, en los lóbulos cardiacos. A la derecha se muestra un corte histológico de pulmón teñido con hematoxilina-eosina (10x) en donde se observa (flechas) una marcada hiperplasia linfoide (acumulación de linfocitos perivascular, peribronquial y peribronquiolar)
El control de la NEP puede realizarse mediante la optimización de las prácticas de manejo y condiciones de alojamiento de los animales, uso de antibióticos y vacunación.La alta prevalencia de la NEP a nivel nacional e internacional y el avance del conocimiento sobre la diversidad genética del microorganismo y sus posibles implicancias en los mecanismos de patogénesis y evasión del sistema inmune de los cerdos, como un retardo en la seroconversión,han devuelto el protagonismo a tan importante patógeno. Desde hace tiempo venimos trabajando en el estudio de la diversidad genética de M. hyopneumoniae en nuestro país. Informamos la existencia de diferentes subtipos genéticos del agente en piaras Argentinas por primera vez en el año 2011 y desde entonces hemos seguido investigando sobre el tema. La idea del presente artículo es presentarlesuna breve actualización acerca de la detección y diversidad genética de M. hyopneumoniaeen nuestro país y en el mundo.
Desde el año 2004 nuestro equipo de trabajo realiza diferentes formatos de PCR para la detección de M. hyopneumoniae a partir de muestras clínicas en animales vivos (hisopado nasal) y animales muertos (lavado traqueo-bronquial). La experiencia en la identificación de este patógeno nos ha permitido avanzar no sólo en su detección, sino también en la identificación de subtipos genéticos.Para estudiar la diversidad genética delM. hyopneumoniae pueden utilizarse varias herramientas moleculares. En nuestro laboratorio nosotros usamos la amplificación por PCR de una región de un gen, llamado p146, que codifica para una adhesina (proteína involucrada en la unión entre el agente y las cilias del pulmón del cerdo). Dentro de la región que analizamos se puede inferir y contabilizar el número de codones que codifican para el aminoácido serina, que se repite en tándem y en base a la cantidad de codones que presenta la secuencia analizada se puede determinar si es el mismo subtipo genético de M. hyopneumoniae o no. Primero se utilizó esta metodología para el estudio de un brote de queratoconjuntivitis en cabras, causado por Mycoplasmaconjunctivae analizando un gen llamado lppS. Luego se identificó un gen homólogo en M. hyopneumoniaey a partir de entonces, la diversidad genética del microorganismo ha sido informada alrededor del mundoutilizando esta metodología.


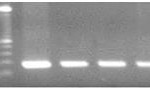
En la foto de la izquierda se observan los productos de la PCR del fragmento del gen p146, corridos en un gel de agarosa. A la derecha se muestra una parte de la secuencia del gen amplificado, en donde pueden visualizarse cada uno de los nucleótidos y puedenidentificarse los motivos de repetición de codones: TCT, TCA y TCC que codifican para el aminoácido serina.
En 2011 encontramos en nuestro país subtipos genéticos del agente entre granjas y dentro de las granjas. Hoy se asume que dentro de cada establecimiento existe una tipología genética predominante pero puede haber otras tipologías menos frecuentes. En el año 2003 se propuso la existencia de cepas de M hyopneumoniaede alta, moderada y baja virulenciay desde entonces el concepto de cepas de alta y baja virulencia es relativamente aceptado alrededor del mundo. Si bien hasta el momento no existe un marcador molecular capaz de discernir entre cepas con mayor o menor virulencia, el conocimiento de la diversidad genética nos acerca a ese hallazgo.
Usando la metodología nombrada anteriormente hemos podido identificar distintos tipos genéticos en las cepas que se usan para vacunas. Esto podría tener implicancias en el uso de las vacunas comerciales según la cepa circulante en cada piara. Refiriéndonos concretamente a M. hyopneumoniae, si bien se ha demostrado que no hay diferencias en la respuesta a la vacunación por parte de los cerdos, según la vacuna (bacterina) fuera fabricada con cepas homólogas (iguales) o heterológas (distintas), o con cepas patógenas o apatógenas, estudios más profundos son necesarios y los antecedentes respecto al tema son realmente bastante escasos.
Según resultados obtenidos en nuestro laboratorio, la amplificación del segmento del gen p146no puede realizarse de cualquier muestra clínica, sino que dan mejores resultados aquellas que contienen alta carga del microorganismo. Por ello, en el trabajo señalado anteriormente (Tamiozzo et al., 2011)realizamos modificaciones a la prueba original propuesta Mayor et al. (2008) que hicieron la técnica más sensible, capaz de tipificar el microorganismo a partir de muestras clínicas con pequeñas cantidades del microorganismo, como un hisopado nasal. Así con una muestra muy fácil de obtener, poco invasiva y sin la necesidad de sacrificar animales puede tipificarse el M hyopneumoniae.Nuestro equipo de trabajo ha podido tipificar al microorganismo antes y después de la aplicación de programas de erradicación de NEP y su aplicación para estudios en brotes es altamente sugerida.

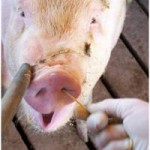
En la foto puede observarse a un operario tomando muestra de hisopado nasal, una muestra poco invasiva, fácilmente obtenible y útil para la tipificación genética de M hyopneumonie.
Actualmente estamos trabajando en el estudio de la sensibilidad de las reacciones de amplificación (PCR) de otras regiones del genoma de M. hyopneumoniae que permitirían una mejor tipificación del microorganismo a partir de hisopados nasales. También estamos caracterizando genéticamente a las bacterinas disponibles comercialmente ya que la información al respecto es bastante escasa y monitoreamos piaras y estudiamos brotes de NEP para un mayor entendimiento del fenómeno.